Des chercheurs simulent des battements de cœur irréguliers pour trouver exactement d’où ils proviennent et réalisent des cœurs virtuels personnalisés qui pourraient améliorer la chirurgie cardiaque.
Dans une étude publiée récemment dans la revue Nature Biomedical Engineering (Computationally guided personalized targeted ablation of persistent atrial fibrillation), information reprise dans un article du magazine IEEE Spectrum (Personalized Virtual Hearts Could Improve Cardiac Surgery), une équipe de chercheurs a réalisé des simulations cardiaques personnalisées pour guider les interventions chirurgicales de 10 patients présentant des battements de cœur irréguliers persistants (fibrillation atriale). Les cœurs virtuels ont prédit où les chirurgiens devraient détruire le tissu cardiaque qui pourrait produire des signaux électriques erratiques maintenant et à l’avenir.
Cette étude de validation de principe ouvre la voie à un essai clinique approuvé par la FDA auprès de 160 patients et qui devrait commencer cet automne. Cet essai permettra de déterminer si la chirurgie virtuelle guidée par le cœur est plus précise et efficace que la procédure classique actuelle à taille unique.
La fibrillation atriale, également appelée fibrillation auriculaire (FA) est le plus fréquent des troubles du rythme cardiaque. Elle fait partie des troubles du rythme supra-ventriculaires. Elle correspond à une action non coordonnée des cellules myocardiques auriculaires, entraînant une contraction rapide et irrégulière des oreillettes cardiaques. La fibrillation atriale est parfois dénommée par abus de langage arythmie ; cependant ce terme est synonyme de trouble du rythme, notion plus large et qui inclut la fibrillation atriale (Source : Wikipedia).
La fibrillation auriculaire (FA) – l’arythmie la plus courante – augmente considérablement le risque d’accident vasculaire cérébral et d’insuffisance cardiaque. Bien que l’ablation par cathéter puisse rétablir des rythmes cardiaques normaux, les patients atteints de FA persistante qui développent une fibrose auriculaire subissent souvent plusieurs échecs d’ablation, ce qui accroît les risques procéduraux.
L’équipe de chercheurs a développé une modélisation informatique personnalisée pour la prédétermination fiable des cibles d’ablation, qui sont ensuite utilisées pour guider la procédure d’ablation chez les patients atteints de FA persistante et de fibrose auriculaire.
L’année dernière, les chirurgiens ont utilisé la simulation virtuelle 3D des ventricules cardiaques de l’équipe Johns Hopkins, les deux grandes cavités inférieures, pour guider la chirurgie de cinq patients dont le rythme cardiaque était plus rapide que la normale. L’équipe de Natalia A. Trayanova
Responsable du Department of Biomedical Engineering de la Johns Hopkins University a également utilisé cette technologie pour identifier les patients à haut risque d’arrêt cardiaque.
La présente étude se concentre sur les signaux électriques anormaux dans les oreillettes – les deux cavités supérieures du cœur – qui provoquent des battements de cœur irréguliers persistants, une affection couramment appelée fibrillation auriculaire (FA). La FA est la cause la plus fréquente de battements de cœur irréguliers et devrait toucher jusqu’à 10 millions d’Américains d’ici 2020.
Les patients peuvent présenter une FA intermittente ou persistante. Dans les deux cas, les médecins pénètrent traditionnellement dans le cœur avec un cathéter et brûlent les tissus entourant les quatre veines pulmonaires de l’oreillette, une région impliquée dans les ratés électriques. L’article explique que la procédure fonctionne bien pour les patients atteints de FA intermittente, mais pas pour ceux atteints de FA persistante, en particulier lorsque les patients ont des cicatrices dans les tissus, qui sont liées à l’âge. Ces patients reviennent souvent en salle d’opération pour des chirurgies répétées, même jusqu’à quatre ou cinq fois, créant à chaque fois davantage de tissu cicatriciel dans le cœur, ce qui peut entraîner davantage de ratés.
La nouvelle procédure individualisée, appelée Optimal Target Identification via Modelling of Arythmythmesis (OPTIMA), pourrait cibler toutes les zones problématiques du cœur lors de la première tentative chirurgicale, y compris celles qui provoqueront des ratés électriques à l’avenir.
Mode d’emploi
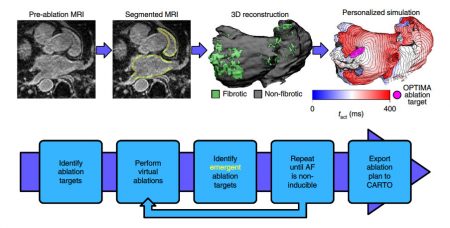
Une patiente atteinte de FA subit des examens du cœur par IRM à contraste renforcé, qui documentent toute cicatrice sur le cœur. Ensuite, les ingénieurs segmentent les images en une représentation géométrique des oreillettes. Dans un programme informatique, ils peuplent cette représentation avec des cellules cardiaques virtuelles. Les cellules se comportent différemment autour des tissus cardiaques normaux ou cicatrisés, de sorte que le cœur numérique adopte progressivement les mêmes comportements que le cœur du patient.

 [Crédit photo : Department of Biomedical Engineering, Johns Hopkins University, Baltimore, MD, USA]
[Crédit photo : Department of Biomedical Engineering, Johns Hopkins University, Baltimore, MD, USA]
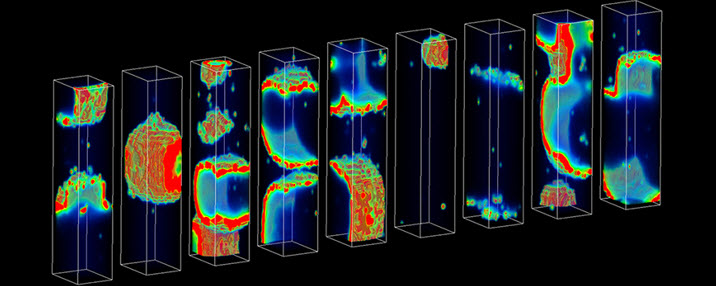
Ensuite, les ingénieurs agissent sur le cœur virtuel avec de petits stimuli électriques pour voir comment il va réagir. Ils regardent et délimitent les zones où un stimulus provoque un rythme cardiaque irrégulier. Ce sont les sites que les chirurgiens devront détruire par brûlage, une procédure appelée l’ablation.
Mais identifier ces sites initiaux ne suffit pas. Après avoir noté toutes les zones de problèmes initiaux, l’équipe effectue une opération virtuelle, détruisant ces zones et ajoutant de nouvelles cicatrices virtuelles, appelées lésions, au modèle. Ensuite, ils refont le test, car de nouvelles cicatrices peuvent entraîner la génération de tissus cardiaques supplémentaires.
Il faut répéter cette opération plusieurs fois pour trouver l’ensemble optimal de lésions, de sorte que le patient ne revienne jamais à l’hôpital après son exécution. Généralement, à partir du troisième tour, il n’ya plus de zones cachées pouvant générer des signaux électriques anormaux.
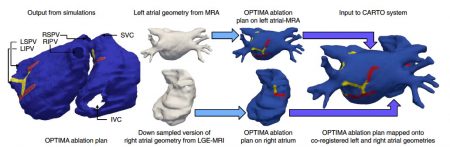
Enfin, une carte électronique du cœur du patient est envoyée au système que les médecins exploitants utilisent lors de la chirurgie, affiché sur des écrans dans la salle d’opération. Le chirurgien utilise cette carte pour guider le cathéter vers les tissus à détruire. Normalement, environ 50% des patients atteints de FA persistante retournent à l’hôpital pour des chirurgies supplémentaires. Sur les 10 patients ayant subi la procédure personnalisée OPTIMA, un seul est revenu pour un traitement supplémentaire.
L’approche personnalisée risque d’être plus coûteuse qu’une intervention chirurgicale classique, car elle implique un examen par IRM. Toutefois, le fait d’empêcher un patient de retourner à l’hôpital pour des procédures supplémentaires peut entraîner des économies globales.
 [Crédit photo : Department of Biomedical Engineering, Johns Hopkins University, Baltimore, MD, USA]
[Crédit photo : Department of Biomedical Engineering, Johns Hopkins University, Baltimore, MD, USA] puis
puis